Содержание
Русское название
Английское название
Baricitinib.
Латинское название вещества Барицитиниб
Baricitinibum.
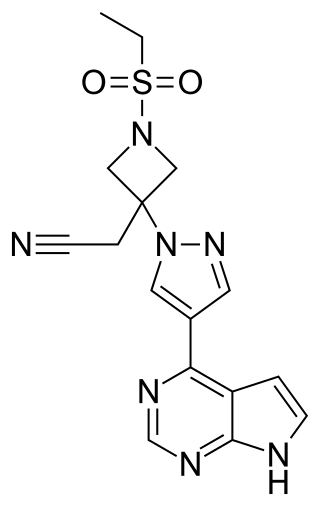
Брутто формула
C16H17N7O2S
Фармакологическая группа вещества Барицитиниб
Иммунодепрессанты.
Нозологическая классификация
- (M06.9) Ревматоидный артрит неуточненный;
Фармакологическое действие
Фармакологическое действие: иммунодепрессивное..
Характеристика
Барицитиниб используют при лечении активного ревматоидного артрита умеренной или тяжелой степени у взрослых пациентов с непереносимостью или отсутствием адекватного ответа на лечение одним или несколькими базисными противоревматическими препаратами.Фармакология
Барицитиниб является селективным и обратимым ингибитором янус-киназы 1 и 2 (JAK1 и JAK2). В исследованиях было показано, что барицитиниб ингибирует активность JAK1, JAK2, тирозинкиназы-2 и JAK3 со значениями IC50 5,9; 5,7; 53 и >400 нМ соответственно.
Янус-киназы (JAK) представляют собой ферменты, которые трансдуцируют внутриклеточные сигналы от клеточных рецепторов ряда цитокинов и факторов роста, участвующих в процессах гемопоэза, воспаления и иммунного ответа. В рамках внутриклеточного сигнального пути JAK фосфорилируют и активируют STAT (транспортеры сигнала и активаторы транскрипции), которые в свою очередь активируют экспрессию гена в клетке. Барицитиниб модулирует эти сигнальные каскады реакций, частично ингибируя ферментативную активность JAK1 и JAK2, тем самым уменьшая фосфорилирование и активацию STAT.
Фармакодинамические эффекты
Ингибирование фосфорилирования STATS, индуцированного ИЛ-6. Применение барицитиниба у здоровых добровольцев приводило к дозозависимому ингибированию фосфорилирования STAT3, индуцированного ИЛ-6, с максимальным ингибированием через 2 ч после применения и возвращением к исходным показателям через 24 ч.
Иммуноглобулины. Через 12 нед после начала применения барицитиниба среднее значение IgG, IgM и IgA в сыворотке крови снижалось и оставалось стабильно сниженным по меньшей мере в течение 104 нед. У большинства пациентов изменение значений Ig находилось в пределах диапазона нормальных значений.
Лимфоциты. В течение 1 нед после начала применения барицитиниба среднее абсолютное число лимфоцитов увеличивалось, однако к 24-й нед возвращалось к исходному значению и в дальнейшем оставалось стабильным в течение по меньшей мере 104 нед. У большинства пациентов изменение числа лимфоцитов находилось в пределах диапазона нормальных значений.
С-реактивный белок. У пациентов с ревматоидным артритом снижение концентрации сывороточного С-реактивного белка наблюдалось уже через 1 нед после начала применения барицитиниба и оставалось сниженным в течение всего периода применения.
Креатинин. Применение барицитиниба приводило к повышению концентрации креатинина в сыворотке крови в среднем на 3,8 мкмоль/л после 2 нед лечения по сравнению с плацебо, в дальнейшем этот показатель оставался стабильным до 104-й нед лечения. Это может быть связано с ингибированием секреции креатинина барицитинибом в почечных канальцах. Следовательно, оценка СКФ на основе определения концентрации креатинина в сыворотке крови может быть несколько ниже без фактического снижения функции почек или возникновения нежелательных реакций со стороны почек.
Вакцинация. Влияние барицитиниба на гуморальный ответ после введения неживых вакцин (инактивированная пневмококковая вакцина или инактивированная противостолбнячная вакцина) было изучено в клиническом исследовании у пациентов с ревматоидным артритом, получавших барицитиниб в дозах 2 и 4 мг. Большинство пациентов, участвовавших в исследовании, получали барицитиниб в комбинации с метотрексатом. Результаты исследования показали, что адекватный иммунный ответ (IgG) развивался у 68% пациентов после введения пневмококковой вакцины и 43,1% пациентов после введения противостолбнячной вакцины.
После перорального приема барицитиниба в диапазоне терапевтических доз наблюдалось дозозависимое увеличение системной экспозиции. Фармакокинетика барицитиниба является линейной по времени.
Всасывание
После перорального приема барицитиниб быстро всасывается, Tmax составляет приблизительно 1 ч (диапазон 0,5–3 ч), абсолютная биодоступность — около 79%. Прием пищи приводил к уменьшению экспозиции барицитиниба на 14%, снижению Сmах на 18% и увеличению Tmax на 0,5 ч. Данные изменения не являются клинически значимыми.
Распределение
Средний Vd после в/в введения составлял 76 л, что свидетельствовало о распределении барицитиниба в тканях. Приблизительно 50% барицитиниба связывается с белками плазмы.
Метаболизм
Метаболизм барицитиниба опосредован изоферментом CYP3A4, при этом биотрансформации подвергается менее 10% полученной дозы. В плазме крови метаболиты барицитиниба не обнаруживались. Фармакологические исследования показали, что барицитиниб выводится преимущественно в неизмененном виде почками (69%) и через кишечник (15%). Почками выводилось 3 метаболита, через кишечник — 1, их количество составляло соответственно около 5 и 1% от введенной дозы. В условиях in vitro барицитиниб является субстратом для изофермента CYP3A4, ОАТ3, P-gp, BCRP и МАТЕ2-К. Барицитиниб может быть ингибитором ОСТ1. Барицитиниб не является ингибитором ОАТ1, ОАТ2, ОАТ3, ОСТ2, ОАТР1В1, ОАТР1В3, BCRP, МАТЕ1 и МАТЕ2-К.
Выведение
Выведение почками посредством КФ и активной секреции через ОАТ3, P-gp, BCRP и МАТЕ2-К является основным механизмом клиренса барицитиниба. В ходе фармакологического исследования было выявлено, что приблизительно 75% вводимой дозы выводилось почками, тогда как только около 20% выводилось через кишечник. У пациентов с ревматоидным артритом средний клиренс и T1/2 составляли в среднем 9,42 л/ч и 12,5 ч соответственно. Сmах и AUC барицитиниба в устойчивом состоянии фармакокинетики у пациентов с ревматоидным артритом были соответственно в 1,4 и 2 раза выше, чем у здоровых добровольцев.
Особые группы пациентов
Почечная недостаточность. Функция почек значительно влияет на экспозицию барицитиниба. Среднее соотношение AUC у пациентов с легкой и умеренной почечной недостаточностью и пациентов с нормальной функцией почек составляет 1,41 и 2,22 соответственно. Среднее соотношение Сmах у пациентов с легкой и умеренной почечной недостаточностью и пациентов с нормальной функцией почек составляет 1,16 и 1,46 соответственно.
Печеночная недостаточность. У пациентов с легкой или умеренной печеночной недостаточностью не обнаружено клинически значимых изменений в фармакокинетике барицитиниба. Применение барицитиниба у пациентов с тяжелой печеночной недостаточностью не изучалось.
Пожилой возраст. Возраст 65 лет и старше или 75 лет и старше не влияет на экспозицию барицитиниба (Сmах и AUC).
Дети. В настоящее время нет данных по безопасности, эффективности и фармакокинетике применения барицитиниба у детей.
Масса тела, пол, раса и этническая принадлежность не оказывают клинически значимого влияния на фармакокинетику барицитиниба.
Применение вещества Барицитиниб
Активный ревматоидный артрит умеренной или тяжелой степени у взрослых пациентов с непереносимостью или отсутствием адекватного ответа на лечение одним или несколькими базисными противоревматическими ЛС (в виде монотерапии или в комбинированной терапии с метотрексатом).
Применение при беременности и кормлении грудью
Было установлено, что каскад реакций JAK/STAT связан с адгезией и поляризацией клеток, что может повлиять на процесс раннего эмбриогенеза. Данные о применении барицитиниба у беременных женщин отсутствуют. В исследованиях на животных была продемонстрирована репродуктивная токсичность. Барицитиниб проявлял тератогенное действие у крыс и кроликов. Согласно результатам исследования на животных, применение высоких доз барицитиниба может оказывать неблагоприятное влияние на внутриутробное развитие скелета.
Применение барицитиниба во время беременности противопоказано. Женщинам детородного возраста следует использовать эффективные методы контрацепции во время и в течение как минимум 1 нед после лечения. В случае, если пациентка забеременела во время применения барицитиниба, ее необходимо проинформировать о возможном риске для плода.
Неизвестно, выделяется ли барицитиниб (или его метаболиты) с грудным молоком.
Данные фармакодинамических/токсикологических исследований на животных показали, что барицитиниб выделяется с грудным молоком. Невозможно исключить риск для новорожденных/младенцев, и поэтому не следует применять барицитиниб в период грудного вскармливания. Необходимо оценить пользу от грудного вскармливания для ребенка и применения барицитиниба для женщины и принять решение о прекращении грудного вскармливания или применения барицитиниба.
Фертильность
Результаты исследований на животных показывают, что применение барицитиниба может снизить женскую фертильность во время лечения. Влияния барицитиниба на сперматогенез не наблюдалось.
Ограничения к применению
Почечная недостаточность с Cl креатинина <30 мл/мин; печеночная недостаточность тяжелой степени; возраст старше 75 лет; активные, хронические или рецидивирующие инфекции (включая туберкулез); снижение числа нейтрофилов (менее 1×109/л); снижение числа лимфоцитов (менее 0,5×109 /л); снижение Hb (<8 г/дл); активная форма вирусного гепатита В и С; одновременное применение живых вакцин; наличие факторов риска развития ТГВ/ТЭЛА; комбинация с биологическими базисными противоревматическими ЛС или другими ингибиторами янус-киназы; комбинация с сильными иммунодепрессантами (например, азатиоприн, такролимус, циклоспорин).
Противопоказания
Повышенная чувствительность к барицитинибу; беременность; период грудного вскармливания; детский возраст до 18 лет (данные по эффективности и безопасности отсутствуют).
Побочные действия вещества Барицитиниб
Инфекции и инвазии: очень часто - инфекция верхних дыхательных путей; часто - опоясывающий лишай, простой герпес, гастроэнтерит, инфекция мочевыводящих путей.
Со стороны системы кроветворения: часто - тромбоцитоз >600×109 клеток/л; нечасто - нейтропения <1×109 клеток/л.
Со стороны обмена веществ: очень часто - гиперхолестеринемия; нечасто - гипертриглицеридемия.
Со стороны пищеварительной системы: часто - тошнота.
Со стороны кожи и подкожных тканей: нечасто - акне.
Прочие: часто - повышение активности АЛТ, АСТ; нечасто - увеличение массы тела, повышение концентрации КФК.
Взаимодействие
При применении барицитиниба в комбинации с мощными иммунодепрессантами, такими как азатиоприн, такролимус или циклоспорин, невозможно исключить риск аддитивной иммуносупрессии.
Применение пробенецида приводило к приблизительно двукратному увеличению AUC(0-∞) без изменения Тmax или Сmax барицитиниба. Следовательно, у пациентов, которые принимают ингибиторы ОАТ3 с сильной ингибирующей активностью, такие как пробенецид, рекомендуемая доза барицитиниба составляет 2 мг 1 раз/сут.
Следует соблюдать осторожность при одновременном назначении лефлуномида или терифлуномида и барицитиниба.
Передозировка
В ходе клинических исследований разовые дозы барицитиниба до 40 мг/сут и многократные дозы до 20 мг/сут в течение 10 дней не оказывали токсического воздействия. Наблюдаемые нежелательные реакции были сопоставимы с теми, которые были зарегистрированы при применении более низких доз, не было выявлено специфической токсичности. Данные фармакокинетического исследования применения однократной дозы 40 мг у здоровых добровольцев показывают, что более 90% вводимой дозы выводится из организма в течение 24 ч. В случае передозировки рекомендуется следить за наличием у пациента признаков и симптомов нежелательных реакций. При развитии нежелательных реакций необходимо проводить соответствующее лечение.
Меры предосторожности
Инфекции
Частота развития инфекций, в частности верхних дыхательных путей, выше при применении барицитиниба, чем при использовании плацебо. У пациентов, которые ранее не получали лечение, применение барицитиниба с метотрексатом приводило к увеличению частоты инфекций по сравнению с монотерапией барицитинибом. У пациентов с активными, хроническими или рецидивирующими инфекциями до начала терапии рекомендуется тщательно оценивать соотношение польза/риск от применения барицитиниба. В случае возникновения инфекции следует обеспечить тщательный контроль состояния пациента, и, если пациент не отвечает на стандартную терапию, рекомендуется временно прекратить применение барицитиниба. Применение барицитиниба не следует возобновлять до разрешения инфекции.
Туберкулез
Перед началом применения барицитиниба пациенты должны пройти скрининг на туберкулез. Барицитиниб не рекомендуется применять у пациентов с активной формой туберкулеза. У пациентов с латентной формой туберкулеза, которые ранее не получали лечение, перед началом терапии барицитинибом необходимо рассмотреть возможность проведения противотуберкулезной терапии.
Отклонения от нормы лабораторных показателей
Согласно данным клинических исследований, менее чем у 1% пациентов были зарегистрированы следующие изменения показателей крови: абсолютное число нейтрофилов менее 1×109/л, абсолютное число лимфоцитов менее 0,5×109/л и Hb менее 8 г/дл. Не рекомендуется начинать терапию или следует временно прекратить применение барицитиниба при снижении числа нейтрофилов менее 1×109/л, лимфоцитов менее 0,5×109/л или Hb менее 8 г/дл.
У пожилых пациентов с ревматоидным артритом увеличивается риск развития лимфоцитоза. Есть данные о редких случаях развития лимфопролиферативных заболеваний.
Реактивация вирусной инфекции
При проведении клинических исследований были зарегистрированы случаи вирусной реактивации, включая реактивацию вируса герпеса (например, опоясывающий герпес, простой герпес). Случаи опоясывающего герпеса чаще наблюдались у пациентов в возрасте 65 лет и старше, которые ранее получали лечение биологическими и традиционными базисными противоревматическими ЛС. При развитии у пациента опоясывающего герпеса применение барицитиниба следует временно прекратить до разрешения заболевания.
В соответствии с клиническими рекомендациями перед началом терапии барицитинибом следует проводить скрининг пациентов для выявления вирусного гепатита. Пациенты с признаками активной формы вирусного гепатита В или С не включались в клинические исследования. Пациенты, у которых обнаруживались антитела к вирусу гепатита С, но не выявлялась РНК вируса гепатита С, были допущены к участию в клинических исследованиях. Также допускалось участие пациентов с антителами к поверхностному и сердцевинному антигенам вируса гепатита В, без поверхностных антигенов вируса гепатита В; у таких пациентов следует проводить мониторинг экспрессии ДНК вируса гепатита В. При выявлении ДНК вируса гепатита В пациент должен быть направлен к гепатологу, чтобы определить возможность продолжения или прекращения терапии.
Вакцинация
Отсутствуют данные о реакции на вакцинацию живыми вакцинами у пациентов, получающих барицитиниб. Не рекомендуется применение живых аттенуированных вакцин во время или непосредственно перед его применением. Иммунизацию рекомендуется провести в соответствии с текущими рекомендациями до начала лечения барицитинибом.
Липиды
У пациентов, получавших барицитиниб, наблюдалось дозозависимое повышение концентрации липидов в крови по сравнению с пациентами, которые получали плацебо. В ответ на применение статинов концентрация ЛПНП снижалась до показателей, зафиксированных перед началом терапии. Липидный профиль следует оценивать примерно через 12 нед после начала применения барицитиниба, после чего лечение пациентов следует проводить в соответствии с международными клиническими рекомендациями по ведению пациентов с гиперлипидемией. Не установлено влияние повышения концентрации липидов на частоту сердечно-сосудистых заболеваний и смертность.
Повышение концентрации трансаминаз печени
При проведении клинических исследований повышение концентрации АЛТ и ACT в 5 раз и более и в 10 раз и более по сравнению с ВГН было зарегистрировано менее чем у 1% пациентов. При совместном применении с метотрексатом у пациентов, которые ранее не получали лечение, отмечалось увеличение частоты повышения концентрации трансаминаз печени по сравнению с монотерапией барицитинибом. При выявлении повышения концентрации АЛТ или ACT во время обследования пациентов и подозрении на лекарственное поражение печени применение барицитиниба следует временно прекратить до тех пор, пока этот диагноз не будет исключен.
Злокачественные новообразования
У пациентов с ревматоидным артритом имеется повышенный риск возникновения злокачественных новообразований, включая развитие лимфомы. Применение иммуномодулирующих ЛС может увеличить риск возникновения злокачественных новообразований, включая лимфому.
Клинических данных для оценки частоты возможного возникновения злокачественных новообразований после применения барицитиниба недостаточно. Долгосрочные исследования оценки безопасности продолжаются.
Тромбоэмболия
Сообщалось о случаях развития ТГВ и ТЭЛА у пациентов, получавших барицитиниб. Следует соблюдать осторожность при его применении у пациентов с факторами риска развития ТГВ/ТЭЛА, такими как пожилой возраст, ожирение, ТГВ/ТЭЛА в анамнезе или перенесших оперативное вмешательство и иммобилизацию. При выявлении клинических признаков ТГВ/ТЭЛА применение барицитиниба следует временно прекратить, немедленно оценить состояние пациента и провести соответствующее лечение.
Мониторинг лабораторных показателей
В следующей таблице приведены лабораторные показатели, подлежащие контролю, и руководство по их мониторингу.
| Лабораторный показатель | Алгоритм действий | Руководство по мониторингу |
| Параметры липидного профиля | Лечение пациентов следует проводить в соответствии с международными клиническими рекомендациями по ведению пациентов с гиперлипидемией | Через 12 нед после начала лечения, а затем в соответствии с международными клиническими рекомендациями по ведению пациентов с гиперлипидемией |
| Абсолютное число нейтрофилов | Если число нейтрофилов менее 1×109 клеток/л, следует прекратить применение барицитиниба, если число нейтрофилов будет выше этого значения, лечение можно возобновить | Перед началом лечения и далее, согласно обычному ведению пациентов |
| Абсолютное число лимфоцитов | Если число лимфоцитов менее 0,5×109 клеток/л, следует прекратить применение барицитиниба, если число лимфоцитов будет выше этого значения, лечение можно возобновить | |
| Hb | При уровне Hb менее 8 г/дл следует прекратить применение барицитиниба, после того, как Hb будет выше этого значения, лечение можно возобновить | |
| Трансаминазы печени | При подозрении на лекарственное поражение печени лечение следует временно прекратить |
Иммунодепрессанты
Не рекомендуется применение барицитиниба в комбинации с биологическими базисными противоревматическими ЛС или другими ингибиторами JAK, т.к. невозможно исключить риск развития аддитивной иммуносупрессии. Данных о применении барицитиниба в комбинации с сильными иммунодепрессантами (например, азатиоприн, такролимус, циклоспорин) недостаточно, поэтому следует соблюдать осторожность при их совместном применении.
Влияние на способность управлять транспортными средствами и работать с механизмами.
Барицитиниб не оказывает или оказывает незначительное влияние на способность управлять транспортными средствами и работать с механизмами.
Способ применения и дозы
Внутрь, 1 раз в сутки, в любое время, независимо от приема пищи.